Содержание
- Научно-производственные подразделения
- Структура института ->
- Производство диагностических сывороток
- СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ХОЛЕРНАЯ О1 АДСОРБИРОВАННАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
- СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ХОЛЕРНАЯ О1 НЕАДСОРБИРОВАННАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
- СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ХОЛЕРНАЯ ОГАВА АДСОРБИРОВАННАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
- СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ХОЛЕРНАЯ ИНАБА АДСОРБИРОВАННАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
- СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ТУЛЯРЕМИЙНАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
- ДИАГНОСТИКУМ ТУЛЯРЕМИЙНЫЙ ЦВЕТНОЙ СУХОЙ ДЛЯ МИКРОРЕАКЦИИ АГГЛЮТИНАЦИИ И РЕАКЦИИ АГГЛЮТИНАЦИИ НА СТЕКЛЕ
- СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ПОЛИВАЛЕНТНАЯ БРУЦЕЛЛЕЗНАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
- ДИАГНОСТИКУМ БРУЦЕЛЛЕЗНЫЙ ЦВЕТНОЙ СУХОЙ ДЛЯ МИКРОРЕАКЦИИ АГГЛЮТИНАЦИИ И РЕАКЦИИ АГГЛЮТИНАЦИИ
- СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ПОЛИВАЛЕНТНАЯ ЛИСТЕРИОЗНАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ НА СТЕКЛЕ
- ДРУГИЕ ПРЕПАРАТЫ ДЛЯ МИКРОБИОЛОГИЧЕСКИХ ЦЕЛЕЙ
- СЫВОРОТКА КРУПНОГО РОГАТОГО СКОТА ЖИДКАЯ ДЛЯ БАКТЕРИОЛОГИЧЕСКИХ ПИТАТЕЛЬНЫХ СРЕД
- КРОВЬ НОРМАЛЬНАЯ БАРАНЬЯ
- Холера (запятая Коха)
- 13.7.1.1. Классификация и общая характеристика семейства Vibrionaceae
- 13.7.1.2. Возбудители холеры
- Вибрионы
- Литература
- Примечания
- Ссылки
- Факторы патогенности холерного вибриона
- Резистентность возбудителей холеры
- Патогенные для человека вибрионы, не относящиеся к виду Vibrio Cholerae
- 86) Холерный вибрион. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- Возбудитель холеры
Научно-производственные подразделения
Структура института ->
-
Производство диагностических сывороток
СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ
ХОЛЕРНАЯ О1 АДСОРБИРОВАННАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
Сухая адсорбированная холерная О1 сыворотка готовится из крови лошадей, полученной после гипериммунизации холерными вибрионами сероваров Инаба и Огава в S-форме, инактивированными нагреванием до 100°С. Сыворотка адсорбирована убитыми Vibrio cholerae non O1. В пробирочной реакции агглютинации титр антител сыворотки с гомологичными культурами составляет 1:1600 или выше, в реакции агглютинации на стекле – не менее 1:100. Препарат применяется для серологической идентификации штаммов Vibrio cholerae O1.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ХОЛЕРНАЯ О1 НЕАДСОРБИРОВАННАЯ СУХАЯ
ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
Сухая неадсорбированная холерная О1 сыворотка готовится из крови кроликов, полученной после гипериммунизации холерными вибрионами сероваров Инаба и Огава в S-форме, инактивированными нагреванием до 100°С. В пробирочной реакции агглютинации титр антител сыворотки с гомологичными культурами составляет 1:1600 или выше, в реакции агглютинации на стекле – не менее 1:100. Препарат применяется для серологической идентификации штаммов Vibrio cholerae O1.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ХОЛЕРНАЯ ОГАВА АДСОРБИРОВАННАЯ СУХАЯ
ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
Сухая холерная диагностическая сыворотка серотипа Огава готовится из крови лошадей, полученной после гипериммунизации холерными вибрионами серовара Огава в S-форме, инактивированными нагреванием до 100°С, с последующей адсорбцией сыворотки убитыми клетками Vibrio cholerae Инаба. В пробирочной реакции агглютинации титр сыворотки с гомологичными культурами составляет не менее 1:400, в реакции агглютинации на стекле – не менее 1:25. Препарат применяется для определения принадлежности холерного вибриона к серовару Огава.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ХОЛЕРНАЯ ИНАБА АДСОРБИРОВАННАЯ
СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
Сухая холерная диагностическая сыворотка серотипа Инаба готовится из крови лошадей, полученной после гипериммунизации холерными вибрионами серовара Инаба в S-форме, инактивированными нагреванием до 100°С, с последующей адсорбцией сыворотки убитыми клетками Vibrio cholerae Огава. В пробирочной реакции агглютинации титр антител сыворотки с гомологичными культурами составляет не менее 1:400, в реакции агглютинации на стекле – не менее 1:25. Препарат применяется для определения принадлежности холерного вибриона к серовару Инаба.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ТУЛЯРЕМИЙНАЯ СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
Сухая диагностическая туляремийная сыворотка готовится из крови лошадей, полученной после гипериммунизации смесью культур трех вирулентных штаммов туляремийного микроба, инактивированного формалином. В пробирочной реакции агглютинации титр антител сыворотки с гомологичными культурами составляет не менее 1:3200, в реакции кольцепреципитации не менее 1:20. Препарат применяется для идентификации туляремийного микроба в пробирочной реакции агглютинации и обнаружения его антигенов в органах павших животных в реакции кольцепреципитации.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
ДИАГНОСТИКУМ ТУЛЯРЕМИЙНЫЙ ЦВЕТНОЙ СУХОЙ
ДЛЯ МИКРОРЕАКЦИИ АГГЛЮТИНАЦИИ И РЕАКЦИИ АГГЛЮТИНАЦИИ НА СТЕКЛЕ
Диагностикум туляремийный цветной лиофилизированный представляет собой взвесь туляремийного микроба, инактивированную формалином и окрашенную гематоксилином. Рабочее разведение препарата не менее 1:16. Препарат в рабочем разведении в микрореакции агглютинации агглютинируется туляремийной диагностической сывороткой до титра антител 1:1280 и выше; цельный диагностикум в реакции агглютинации на стекле – в разведении 1:10. Препарат применяется для обнаружения туляремийных антител в сыворотках крови людей и животных.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ПОЛИВАЛЕНТНАЯ БРУЦЕЛЛЕЗНАЯ СУХАЯ
ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ
Сухая бруцеллезная диагностическая сыворотка готовится из сыворотки крови кроликов, гипериммунизированных бруцеллами вакцинного штамма B. abortus 19ВА в S-форме, инактивированными нагреванием до 100°С или добавлением формалина. В пробирочной реакции агглютинации титр антител сыворотки с гомологичными культурами составляет не менее 1:1600, в реакции агглютинации на стекле – не менее 1:25. Препарат применяется для идентификации бруцелл.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
ДИАГНОСТИКУМ БРУЦЕЛЛЕЗНЫЙ ЦВЕТНОЙ СУХОЙ
ДЛЯ МИКРОРЕАКЦИИ АГГЛЮТИНАЦИИ И РЕАКЦИИ АГГЛЮТИНАЦИИ
Диагностикум бруцеллезный цветной лиофилизированный представляет собой взвесь бруцеллезного микроба, инактивированную формалином и окрашенную гематоксилином. Рабочее разведение препарата не менее 1:16. Препарат в рабочем разведении в микрореакции агглютинации и пробирочной реакции агглютинации агглютинируется бруцеллезной диагностической сывороткой до титра антител 1:800 и выше; цельный диагностикум в реакции агглютинации на стекле (Хеддльсона) агглютинируется на четыре креста в сыворотке объемом 0,04, 0,02 и 0,01 мл. Препарат применяется для выявления специфических антител в сыворотке крови больных бруцеллезом людей и животных.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
СЫВОРОТКА ДИАГНОСТИЧЕСКАЯ ПОЛИВАЛЕНТНАЯ ЛИСТЕРИОЗНАЯ
СУХАЯ ДЛЯ РЕАКЦИИ АГГЛЮТИНАЦИИ НА СТЕКЛЕ
Сухая листериозная диагностическая сыворотка готовится из крови кроликов, гипериммунизированных культурой вирулентного штамма Listeria monocytogenes, инактивированной нагреванием до 100°С. В реакции агглютинации на стекле титр антител сыворотки с гомологичной культурой составляет не менее 1:100. Препарат применяется для идентификации возбудителя листериоза.
Срок годности 5 лет.
Форма выпуска: ампулы по 1 мл.
ДРУГИЕ ПРЕПАРАТЫ ДЛЯ МИКРОБИОЛОГИЧЕСКИХ ЦЕЛЕЙ
Сыворотка лошадиная нормальная готовится из крови лошади. Сыворотка не содержит консерванта. Препарат предназначен для добавления в питательные среды, применяемые для выделеия и культивирования микроорганизмов (коринебактерий, нейссерий, стрептококков и др.) при диагностике соответствующих инфекций и может использоваться при определении токсигенности дифтерийного микроба.
Срок годности 2 года.
Форма выпуска: флаконы по 40 мл.
СЫВОРОТКА КРУПНОГО РОГАТОГО СКОТА ЖИДКАЯ
ДЛЯ БАКТЕРИОЛОГИЧЕСКИХ ПИТАТЕЛЬНЫХ СРЕД
Сыворотка не содержит консерванта. Препарат предназначен для добавления в бактериологические питательные среды, применяемые для культивирования микроорганизмов (коринебактерий, нейссерий, стрептококков и др.) при диагностике соответствующих инфекций. Может использоваться при определении токсигенности дифтерийного микроба.
Срок годности 2 года.
Форма выпуска: флаконы по 40 мл.
КРОВЬ НОРМАЛЬНАЯ БАРАНЬЯ
Препарат представляет собой дефибринированную кровь барана. Кровь не содержит консерванта.
Срок годности 2 года.
Форма выпуска: флаконы или пробирки от 5 мл до 200 мл.
Холера (запятая Коха)
История открытия возбудителя холеры.
В 1883 г. Р. Кох во время эпидемии холеры в Индии выделил и изучил биологические свойства классического холерного вибриона, в 1906 г. супруги Готшлих открывают биовар V. eltor на карантинной станции Эльтор в Египте при обследовании трупов погибших от «дизентерии» паломников (до 1961 г. – спор о том, а является ли V. еltor возбудителем холеры, но в 1961 г. в Индонезии – вспышка холеры, вызванная данным биоваром); в 1993 г. во время вспышки холеры в юговосточной Азии обнаружили вибрион серогруппы О139 (Бенгал).
Распространение холеры.
I период (до 1817 г.) – заболеваемость холерой не выходила за пределы Индии с эпицентром в дельте рек Ганг и Брахмапутра.
II период (1817-1926 гг.) – с развитием торговли по караванным путям купцов холера проникает за пределы Индии на другие страны и континенты, вызывая 6 пандемий. В России с 1823 по 1926 годы переболело 5,6 млн. человек, из них погибли более 2 млн. (около 40%).
III период (1926-1961 гг.) – отмечается снижение заболеваемости холерой во всем мире (спородические случаи в Индии и Африке).
IV период (1961 г. – настоящее время) – 7 пандемия холеры.
Особенности 7 пандемии холеры:
v берет свое начало не из Индии, а из Индонезии (остров Сулавеси);
v распространяется в две волны: 1 – до 1991 года (Индонезия); 2 – с 1991 года (охватывает страны Южной и Северной Америки);
v высокая скорость распространения (за первые 10 лет охватила 72 страны, в 1970 г. первые случаи в СССР – Керчь, Астрахань, Одесса и распространилась по стране, в 1970 г. в Кировской области – 6 заболевших и 2 носителя, а в 1974 г. – более 200 заболевших и носителей, 6 летальных исходов, начиная с 90-х годов прошлого столетия холера «бродит» по югу России – Ростовская область, Чеченская республика и Дагестан, в раннее жаркое лето может достичь и северных регионов);
v более продолжительна;
v смена биовара V. cholerae asiaticae на V. eltor;
v высокий процент формирования вибрионосительства;
v течение болезни в виде стертых, атипичных форм.
Таксономия:
Семейство: Vibrionaceae
Род: Vibrio
Вид: V. cholerae
Биовары: V. cholerae cholerae (asiaticae, classicae)
V. cholerae eltor
V. cholerae bengalii (О139)
Всего род Vibrio включает 36 видов (V. parahaemolyticus, V. vulnificus, V. metschnigovii, V. proteus, V. albensis, V. alginoluticus, V. mimicus, V. damsela… – возбудители холероподобных заболеваний)
Морфология и тинкториальные свойства.
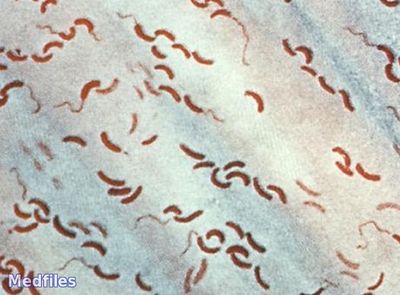
Слегка изогнутые грамотрицательные палочки (хорошо окрашиваются анилиновыми красителями) средних размеров (0,2-0,4×1,5-4 мкм), монотрих (жгутик в 2-3 раза длиннее тела, повышенная подвижность, снаружи покрыт оболочкой, образованной выростом наружного слоя клеточной стенки и напоминающей ундулирующую мембрану), спор и капсул не образует. В старых культурах – полиморфны (кокковидные и нитевидные формы). В мазках из нативного материала располагаются в виде «стайки рыб». При лечении антибиотиками подвижность уменьшается и может превращаться в L-формы.
Культуральные свойства.
Строгий аэроб (факультативный анаэроб, но лучше растет в аэробных условиях), хемоорганогетеротрофы, оптимальная температура роста 370С, время культивирования – 6-24 часа, хорошо растет на обычных питательных средах, но требователен к pH (галофил), оптимальная pH 8,0-9,0. В 1% щелочной пептонной воде через 6-8 часов отмечается рост в виде нежной, тонкой, голубоватой пленки (при встряхивании разрушается). На плотной среде (щелочной агар) через 10-12 часов вырастают мелкие (1,5-2 мм), маслянистые, гладкие, прозрачные, голубоватые колонии с ровным краем (S-формы). При длительном культивировании колонии увеличиваются в размерах, становятся мутными, с плотным центром, пигментированные (коричневого или желтого цвета), шероховатые (R-формы), бактерии из них не чувствительны к бактериофагам, антибиотикам и не агглютинируются О-сывороткой. На щелочно-кровяном агаре V. eltor дает зону гемолиза. На ТСBS-агаре (с тиосульфатом, цитратом, солями желчных кислот и сахарозой) образуют желтые колонии.
Биохимические свойства.
Активны, оксидазоположительны, V. cholerae eltor и V. cholerae bengalii могут давать положительную реакцию Фогеса-Проскауэра, расщепляют многие сахара (глюкозу, лактозу, мальтозу, маннит, гликоген, крахмал…) с образованием кислоты без газа. По способности ферментировать сахарозу, арабинозу и маннозу все вибрионы по классификации Хейберга разделены на 6 групп. Холерные вибрионы принадлежат к 1 группе – расщепляют сахарозу, маннозу и не расщепляют арабинозу. Также не сбраживают рамнозу, дульцит, инулин, инозит. Разжижают желатин в виде воронки, образуют индол, разлагают мочевину до аммиака, восстанавливают нитраты в нитриты, свертывают кроличью плазму, разжижают свернутую сыворотку, молоко. Н2S не образуют.
Антигенная структура.
v О-антиген – группо- и типоспецифический, термостабильный ЛПС КС. В роду Vibrio по О-антигену выделяют более 200 серогрупп. Холерный вибрион относится к О1 и О139 группам. Внутри О1 группы О-антиген неоднороден и включает три компонента – А, В и С, по сочетанию которых выделяют три серотипа: АВ – Огава (Ogava), АС – Инаба (Inaba), АВС – Гикошима (Hicoshima). Вибрионы, не агглютинирующиеся сыворотками групп О1 и О139, называются неагглютинируемыми – НАГ вибрионами, вызывают холероподобные заболевания.
v Н-антиген – термолабильный, общий, белковой природы.
v Эндотоксин – стимулирует выработку вибриоцидных антител.
v Холероген – запускает синтез антитоксических антител.
Факторы патогенности.
Токсины:
v Эндотоксин – ЛПС клеточной стенки, термостабильный, вызывает местное воспаление в тонком кишечнике, его сокращение (запускает каскад арахидоновой кислоты, что приводит к синтезу простагландинов E, F) и индуцирует синтез антител.
v Экзотоксин=энтеротоксин=холероген (основная роль в патогенезе) – термолабильный белок, состоит из двух компонентов: А и В. Компонент В – нетоксичный, обладает способностью соединяться с рецепторами эпителиальных клеток тонкого кишечника, облегчая проникновение в клетку компонента А. Компонент А составляют субъединица А1 (активный центр) и субъединица А2, связывающая А и В. Субъединица А1 активирует внутриклеточную аденилатциклазу, приводя к увеличению внутриклеточного содержания цАМФ и выходу жидкости и электролитов из клеток либеркюновых желез в просвет кишечника.
Ферменты патогенности:
v Нейраминидаза;
v Гиалуронидаза;
v Муциназа;
v Протеазы;
v Лецитиназа;
v Гемолизин V. eltor.
Структурные и химические компоненты клетки:
v Пили I типа;
v Жгутик, обусловливающий движение, а также преодоление слизистого слоя и взаимодействие с эпителиальными клетками;
v Фактор G – фактор проницаемости.
Резистентность.
Выживаемость во внешней среде зависит от pH среды, вибрионы чувствительны к действию прямых солнечных лучей, высокой температуре (при 500С погибают за 30 минут, 1000С – через несколько секунд), высушиванию. В открытых водоемах сохраняются от нескольких дней до 3 месяцев, в почве от 8 дней до 3 месяцев, в выгребных ямах – до 3-4 месяцев, в морской воде до 47 суток, в сточных водах – 1-2 суток. Сохраняются в молоке и молочных продуктах от 5 дней до 4 недель, на фруктах 1-2 дня, на сырых овощах – 2-4 дня. Устойчивы к действию низких температур (во льду могут сохраняться до 1-4 месяцев). Высокочувствительны к кислотам (KMnO4 – 15 минут), хлорсодержащим дезсредствам (10 минут), антибиотикам тетрациклинового ряда, V. eltor устойчив к полимиксину в отличие от V. cholerae asiaticae.
Роль в патологии.
Холера – острое инфекционное особо-опасное заболевание с тенденцией к эпидемическому и пандемическому распространению, протекающее по типу острого гастроэнтерита с резким нарушением водно-солевого обмена, сопровождающееся обезвоживанием и тяжелой интоксикацией.
Эпидемиология.
Антропоноз.
Источник инфекции – больной человек или вибриононоситель.
Механизм заражения: фекально-оральный (пути – водный, алиментарный, контактно-бытовой). Определенную роль в распространении холеры играют мухи.
Патогенез и клинические особенности.
Входные ворота – тонкий кишечник, основная роль принадлежит холерогену, вызывающему дегидратацию и обессоливание организма. Вибрион находится только в тонком кишечнике, размножается, не распространяясь по организму, вибрионемия отсутствует.
Инкубационный период – от нескольких часов до 2-3 дней.
Клинические периоды холеры:
1. Холерный энтерит: на фоне нормальной температуры редкий жидкий стул, боли в животе, тенезмы, через 1-2 дня присоединяется рвота.
2. Острый гастроэнтерит: частая рвота, урчание в животе, испражнения приобретают вид «рисового отвара» (мутная жидкость с плавающими остатками слизи и клетками эпителия), акты дефекации учащаются (выделяют до 30 литров в сутки), язык покрывается налетом, количество мочи уменьшается, выраженная жажда, обезвоживание.
3. Холерный алгид – t 35C, кожные покровы серые, синюшные, морщинистые, лицо Гиппократа (facies hippocratica): нос заострен, глаза запавшие, выступающие скулы, афония, гипотония. Смерть наступает от сердечно-сосудистой и почечной недостаточности в результате обезвоживания и интоксикации.
Иммунитет.
Постинфекционный иммунитет – напряженный, непродолжительный, антимикробный и антитоксический.
Микробиологическая диагностика.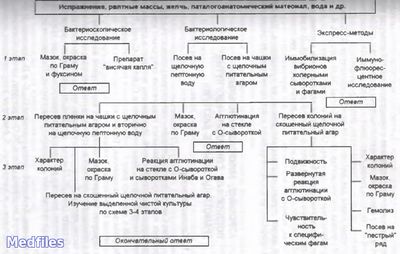
Исследуемый материал – фекалии, рвотные массы, желчь, секционный материал, мухи, пищевые продукты, вода, ил, гидробионты, сточные воды.
1. Бактериоскопический метод.
2. Бактериологичекий метод (основной).
3. Экспресс-методы – РИФ, реакция иммобилизации вибрионов О1-сывороткой и бактериофагом, ПЦР.
4. Серологический метод – РА, РПГА, РИФ, ИФА.
Предварительный положительный ответ при диагностике холеры выдается через 5-6 часов на основании обнаружения в посевах культур, агглютинирующихся на стекле холерной О1-сывороткой (в разведении не менее 1:100) и положительном результате ускоренных методов исследования.
Окончательный положительный ответ выдается через 18-48 часов на основании выделенных культур, имеющих типичные морфологические признаки с учетом данных развернутой реакции агглютинации с холерными сыворотками О1, Огава, Инаба, пробы с холерными диагностическими фагами, принадлежности к 1 группе Хейберга.
Профилактика.
Неспецифическая: раннее выявление больных и носителей, усиление санитарно-гигиенического надзора, санитарно-просветительская работа, введение карантинных мероприятий.
Специфическая – вакцинация по эпидемиологическим показаниям одной из вакцин:
v холероген-анатоксин;
v холероген-анатоксин в сочетании с О-антигеном холерного вибриона Инаба и Огава;
v химическая вакцина из штаммов классического вибриона и V. eltor (химическая бивалентная таблетированная вакцина);
v убитая вакцина из штаммов Огава и Инаба или штаммов вибриона Эль-Тор.
>13.7. Патогенные вибрионы
13.7.1.1. Классификация и общая характеристика семейства Vibrionaceae
В настоящее время семейство Vibrionaceae включает 8 родов бактерий. Основные патогенные представители относятся к роду Vibrio
Ведущую роль в патологии человека играет возбудитель холеры V. сholerae.
V. рarahaemolyticus является причиной диарейных инфекций, V. vulnificus иногда способен вызывать раневую инфекцию и септицемию.
По морфологии возбудители представляют собой изогнутые подвижные палочки размерами 2-4 мкм. Спор не образуют.
Вибрионы распространены повсеместно: обитают в морской и пресной воде, часто колонизируют организмы водных животных (амфибий, ракообразных, рыб и др.)
Температурный оптимум для многих видов 37°С (некоторые возбудители, обитающие в морской воде, лучше размножаются при температуре 25°С и ниже).
При культивировании вибрионов в среду вносят 2-3% раствор NaCl (галотолерантные микроорганизмы).
Данные бактерии – хемоорганотрофы с окислительным и бродильным типом метаболизма.
Ферментируют глюкозу и другие углеводы с образованием кислоты, иногда газа. Оксидазоположительны.
13.7.1.2. Возбудители холеры
Заболевание известно с древних времен. До 1817 г. холера вызывала эпидемии в странах Юго-Восточной Азии (в районах рек Ганга и Брахмапутры). С 1817 г. по 1926 г. наблюдалось распространение болезни за пределы эпидемических очагов с развитием пандемий почти на всех континентах.
В 1883 г. Р. Кох открыл возбудителя холеры – классический холерный вибрион. В 1906 г. Ф. Готшлихт на карантинной станции Эль-Тор выделил еще один биовар возбудителя – вибрион Эль-Тор. В течение XIX века было зарегистрировано 6 эпидемий холеры, последняя из которых завершилась в 1923 г.
В 1961 г. развилась 7 пандемия холеры с преобладанием вибриона Эль-Тор. В начале 1993 г. появились данные о вспышках холеры в Юго-Восточной Азии, вызванных вибрионами неизвестной ранее серогруппы О139 (Бенгал). Считается, что этот вариант становится возбудителем 8 пандемии холеры, хотя вибрион Эль-Тор также продолжает выделяться от больных. В частности, он стал причиной эпидемии холеры на Гаити в 2010 г.
Морфология
Холерные вибрионы представляют собой изогнутые палочки размерами 2-4 мкм, имеют один или два полярных жгутика. Вибрионы весьма подвижны.
Спор не имеют. Продуцируют экзополисахарид, который участвует в формировании микробной биопленки. Представители серогруппы О139 образуют капсулу.
Бактерии обладают полиморфизмом. Типичный возбудитель в форме «запятой» обычно наблюдают в образцах клинического материала. В мазках из колоний преобладают палочковидные возбудители. Иногда возникают нитевидные, кокковидные, булавовидные формы. Под действием пенициллина могут превращаться в L-формы.
Хорошо окрашиваются многими анилиновыми красителями, грамотрицательны.
Культуральные свойства
Растут на простых питательных средах в температурном диапазоне 16-40°С, оптимум – 37°С, селективными являются щелочные среды с рН 7,6-9,0.
На жидких средах вызывает помутнение и образование нежной голубоватой пленки на поверхности. На 1% щелочной пептонной воде (рН 8,8-9,0) растут быстро, помутнение и пленка появляется через 6-8 часов.
На твердых средах (щелочной агар) образуют мелкие, прозрачные, с ровными краями, голубоватые в проходящем свете колонии.
На агаре с тиосульфатом, цитратом, солями жёлчных кислот, сахарозой и индикатором бромтимоловым синим (ТЦБС-агар) образуют желтые колонии на фоне голубовато-серой среды. На среде Монсура (щелочной таурохолат-теллурит-желатиновый агар) растут в виде серо-черных колоний.
Биохимические свойства
Факультативный анаэробы с более выраженными аэробными свойствами.
Холерные вибрионы биохимически весьма активны. Ферментируют с образованием кислоты глюкозу, сахарозу, мальтозу, маннозу, маннит, крахмал, не разлагают лактозу. По отношению к трем углеводам – маннозе, сахарозе и арабинозе – все вибрионы разделяют на 6 групп по Хейбергу.
Холерные вибрионы разлагают маннозу и сахарозу, не разлагают арабинозу и принадлежат к 1 группе Хейберга.
Проявляют протеолитическую активность: разжижают желатину в виде воронки, гидролизуют казеин. Обладают плазмокоагулирующим и фибринолитическим действием. Свертывают молоко, разлагают белки до индола и аммиака. Восстанавливают нитраты в нитриты.
На основании биологических различий холерные вибрионы разделяют на 2 биовара: классический и Эль-Тор. Особенностью вибриона Эль-Тор является способность гемолизировать эритроциты, в связи с чем его относят к гемолитическим вибрионам. Дифференциальные различия возбудителей холеры представлены в табл. 13.
Таблица 13.
Дифференциальные признаки возбудителей холеры
|
Признак |
V. cholerae, классический биовар |
V. cholerae, биовар Эль-Тор |
Серогруппа О139 |
|
Гемолиз эритроцитов барана |
— |
+ |
— |
|
Реакция Фогеса-Проскауэра |
± (чаще –) |
± (чаще +) |
± (чаще +) |
|
Чувствительность к полимиксину В (50ЕД) |
+ |
— |
— |
|
Агглютинация куриных эритроцитов |
— |
± (чаще +) |
± (чаще +) |
|
Чувствительность к классическому монофагу |
+ |
— |
— |
|
Чувствительность к монофагу Эль-Тор |
— |
+ |
Антигенная структура
У холерных вибрионов есть термостабильный О-антиген и термолабильный жгутиковый Н-антиген. Жгутиковый Н-АГ является общим.
По структуре О-АГ выделяют до 200 серогрупп. Оба биовара возбудителей холеры относятся к серогруппе О1.
Было установлено, что О1-АГ неоднороден и состоит из трех субъединиц: А, В, С, по которым различают серовары АВ – Огава, АС – Инаба и АВС – Гикошима. Эти свойства являются эпидемиологическими маркерами данных возбудителей.
Представители серогруппы О139 не агглютинируются О1-сыворотками. Данный вариант произошел от биовара Эль-Тор.
Его возникновение обусловлено генетическими механизмами. В результате рекомбинации возбудитель приобрел группу генов, кодирующих новый вариант ЛПС клеточной стенки совместно с полисахаридом капсулы.
Значительные изменения в строении поверхностных АГ обеспечили «ускользание» бактерий серогруппы О139 от действия факторов иммунитета, направленных к другим возбудителям холеры.
Другие вибрионы, которые также не агглютинируются О1-сывороткой, обозначаются как НАГ-вибрионы (или неагглютинирующиеся). Они способны вызывать самостоятельные диарейные заболевания.
Факторы вирулентности
Возбудитель содержит многочисленные адгезины и факторы колонизации. К ним относятся гемагглютинин и различные виды пилей.
Экзополисахарид вибрионов выполняет защитную функцию и обеспечивает образование биопленки.
Основную роль в патогенезе холеры играет экзотоксин (или холероген) – термолабильный белок, устойчив к действию протеолитических ферментов, разрушается фенолом и формалином. По механизму действия представляет собой энтеротоксин.
Молекула экзотоксина состоит из 2 компонентов (А и В) общей молекулярной массой 84 кД.
Рецепторный компонент В имеет 5 субъединиц. Он взаимодействует с GМ1-ганглиозидным рецептором на энтероцитах и обеспечивает проникновение в клетку токсического компонента А. В клетке происходит восстановление компонента А с образованием субъединицы А1, которая катализирует рибозилирование клеточного G-белка.
В результате активируется аденилатциклаза, и происходит повышение уровня цАМФ в энтероцитах. Это приводит к активной секреции ионов хлора и бикарбонатов, подавлению всасывания ионов натрия, хлора и воды, выходу жидкости и электролитов из железистых клеток в просвет кишечника с развитием тяжелой диареи.
Образование токсина определяется ctx-генами трансдуцирующего CTXφ -бактериофага. Попадание фага CTXφ в холерный вибрион и его интеграция в геном приводят к лизогенной конверсии возбудителя, и вибрион получает способность к синтезу холерного токсина.
Однако успешная трансдукция фага в бактерии возможна только при наличии у вибрионов особых рецепторных пилей. Они способны специфически связывать CTX-фаг, обеспечивая его проникновение в клетку.
Рецепторные пили кодируются генами отдельного генетического острова патогенности VPI. Предполагается, что данный остров патогенности попадает в холерный вибрион в результате трансдукции еще одного специфического фага VPIφ.
Ферменты агрессии и инвазии гиалуронидаза и нейраминидаза разжижают слизь, облегчают доступ бактерий к эпителию, обеспечивают взаимодействие с микроворсинками.
Полисахарид капсулы бактерий серогруппы О139 защищает от фагоцитоза и предохраняет от действия АТ и комплемента.
Резистентность
Холерные вибрионы устойчивы к низким температурам – во льду жизнеспособны до 1 месяца. В морской воде сохраняются до 1,5-2 месяцев, в речной – до нескольких недель, в почве – до 3 месяцев, в фекалиях – до 3 суток. В вареных продуктах, молоке и молочных продуктах, сырых овощах жизнеспособны 2-5 дней, на фруктах – 1-2 дня.
Вибрионы обладают слабой резистентностью к действию повышенной температуры. При 80°С погибают через 5 мин, при 100°С – мгновенно. Холерные вибрионы высокочувствительны к высушиванию, ультрафиолетовому облучению, хлорсодержащим препаратам; все вибрионы высокочувствительны к кислотам.
Патогенез и характеристика заболевания
Возбудитель является нормальным обитателем водной среды в странах Юго-Восточной Азии, особенно в слабосоленых водах эстуариев и дельт рек, теплой прибрежной морской зоне. Он прикрепляется к зоопланктону, образует биопленку, при этом долго сохраняет жизнеспособность.
В благоприятных условиях при совместном обитании между возбудителями происходит горизонтальный перенос различных генов, включая гены патогенности.
Исходно непатогенный холерный возбудитель приобретает вирулентность после нескольких этапов генетической рекомбинации, в основе которой лежит трансдукция бактериофагов.
Первоначально он приобретает способность к синтезу пилей – специфических рецепторов к CTXφ-бактериофагу. После этого происходит трансдукция CTXφ-фага, содержащего гены экзотоксина-холерогена. После встраивания фага в геном возбудитель холеры становится высоковирулентным.
Холера – это острое антропонозное особо опасное инфекционное заболевание, протекающее с глубокой дегидратацией и деминерализацией (потерей воды и солей) в результате диареи и рвоты.
Болезнь по-прежнему представляет собой серьезную эпидемиологическую угрозу, особенно для развивающихся стран. Во время эпидемии 2010-2011 г.г. после землетрясения на Гаити и в сопредельных странах заболело более 250 тыс. человек, из них более 4500 умерло. Летальность составила около 2%. При этом среди госпитализированных больных с тяжелым течением заболевания летальность может быть существенно выше.
Отдельные случаи заболевания регистрируются на территории СНГ (вспышка на Украине 2011 г.)
Резервуар и источники инфекции – больные и бактерионосители.
Основной механизм заражения – фекально-оральный, который реализуется водным, алиментарным и контактно-бытовым путями. Определенную роль играют мухи, способные переносить возбудителя с испражнений на пищевые продукты.
Ведущим путем передачи, приводящим к эпидемиям, является водный. Заражение происходит как при питье инфицированной воды, так и при использовании ее для мытья овощей, фруктов и во время купания. Недостаточная термическая обработка продуктов приводит к заражению. Как и при других кишечных инфекциях, заболеваемость холерой увеличивается в летне-осенний период.
Инфицирующая доза для возбудителя холеры биовара Эль-Тор при заражении через воду высока – 106-1010 микробных клеток. Однако при алиментарном заражении, особенно для лиц с пониженной кислотностью желудочного сока, с анацидными гастритами доза возбудителя существенно ниже – 102-104 бактерий.
Попадающие через рот с водой или пищей холерные вибрионы в большинстве своем погибают под действием кислой среды желудка. Оставшиеся возбудители проникают в тонкую кишку, локализуются в просвете кишечника и прикрепляются к микроворсинкам эпителия при помощи адгезинов.
Выделение эпителиальными клетками щелочного секрета, высокое содержание пептонов и желчи способствуют интенсивному размножению холерного вибриона и продукции экзотоксина. При этом холера – неинвазивная инфекция. Возбудитель внутрь клеток не проникает и воспалительная реакция не развивается.
Действие выделяемого вибрионом экзотоксина приводит к гиперсекреции ионов хлора, других электролитов и воды из энтероцитов в просвет тонкой кишки. Наряду с этим снижается реабсорбция воды в толстом кишечнике. Это обусловливает основные клинические проявления холеры: водянистую диарею и рвоту. В результате обезвоживания и нарушения электролитного баланса развиваются гиповолемия со сгущением крови и нарушением микроциркуляции, что приводит к артериальной гипотензии, сердечной недостаточности, нарушению сознания и гипотермии.
Инкубационный период колеблется от нескольких часов до 5 дней (в среднем 2-3 дня). Заболевание может развиваться в типичной и атипичной формах.
При типичном течении в зависимости от степени дегидратации различают легкую, среднетяжелую и тяжелую формы холеры. В типичных случаях болезнь развивается остро, часто внезапно. Появляются позывы на дефекацию, диарея (от 3 до 15-20 раз в сутки) и рвота. Стул обычно обильный, водянистый, напоминает «рисовый отвар». Рвота «фонтаном», без тошноты, многократная, с примесью желчи. В тяжелых случаях человек теряет до 30 л воды в сутки, температура тела снижается до 35-34°С (холерный алгид – от лат. аlgus – холодный).
Отмечается характерное появление facies hippocratica (запавшие глаза с заостренными чертами лица). При отсутствии лечения летальность больных в алгидной стадии достигает 60%.
В современных условиях большинство случаев холеры вызваны вибрионом Эль-Тор и протекают в легкой форме. Соотношение тяжелых поражений к количеству легких, стертый форм для классической холеры составляет 1:5-10, для холеры Эль-Тор 1:25-100.
Иммунитет
После перенесенного заболевания прочный, длительный, повторные случаи наблюдаются редко. Он обусловлен антитоксическими и антимикробными антителами, клетками иммунной памяти и фагоцитами.
Лабораторная диагностика
Основной метод – бактериологический. С учетом эпидемиологической опасности заболевания идентификация возбудителя должна происходить в максимально короткие сроки.
Целью исследований является выявление больных и бактерионосителей, контроль за эффективностью лечения больных и санация носителей, контроль над объектами внешней среды и эффективностью дезинфекционных мероприятий.
Материалы для исследований – испражнения, рвотные массы, желчь, секционный материал, вода, смывы с объектов окружающей среды, пищевые продукты и др.
Материал следует доставлять в лабораторию не позже 2 ч после забора. При невозможности образцы помещают в транспортные среды (наиболее пригодна 1% пептонная вода с рН 8,2-8,6). Для посева используют жидкие среды обогащения, щелочной МПА, элективные среды (ТЦБС-агар и др.)
Срок роста на щелочной пептонной воде 6-8 ч, на щелочном агаре не менее 14-16 ч, на элективных плотных средах 18-24 ч.
Исследование больных, бактерионосителей и трупного материала проводят в несколько этапов.
Первоначально материал засевают на накопительную среду (например, щелочную пептонную воду), на щелочной агар или среду ТЦБС).
После инкубации в течение 6-8 часов на щелочной пептонной воде образуется пленка микроорганизмов. Из нее готовят препараты для нативной микроскопии и окраски по Граму. Обнаруживают грамотрицательные вибрионы, обладающие выраженной подвижностью. Ставят тест на оксидазу, который должен быть положительным. Проводят реакцию агглютинации с О1-и О139-сыворотками в титре 1/100. При наличии агглютинации дают предварительный положительный ответ о выделении возбудителя.
Из материала среды производят высев на щелочной агар и вторую среду накопления. Если при исследовании материала ускоренными методами (микроскопия, агглютинация О1-сывороткой) получают положительные результаты, пересев на другую среду накопления не производят.
Далее из чашек с ростом возбудителей отбирают для исследования не менее 5 подозрительных колоний. При этом на среде ТЦБС образуются колонии желтого цвета вследствие разложения сахарозы. Проверяют морфологию бактерий, проводят оксидазный тест. Подозрительные колонии исследуют в реакции агглютинации на стекле с О1-антисывороткой, с сыворотками Инаба и Огава в разведении 1:50-100, а также холерной сывороткой О139.
Материал колоний пересевают для выделения чистой культуры на скошенный щелочной агар или среды с сахарозой и индикатором. Затем проводят серологическую и биохимическую иидентификацию выросших микроорганизмов, дифференцируют биовары возбудителей холеры по специфическим тестам, включая фаготипирование.
Для ускоренной идентификации возбудителей можно применять метод иммунной флюоресценции.
Лечение
Основным направлением в лечении является немедленное восполнение дефицита воды и электролитов. Адекватная регидратация и реминерализация солевыми растворами с глюкозой, заместительная инфузионная терапия позволяют стабилизировать состояние больных и приводят к выздоровлению.
Антибактериальную терапию проводят препаратами тетрациклинового ряда. Можно использовать хлорамфеникол, фторхинолоны.
Профилактика
С целью специфической профилактики используются вакцины.
Вакцина холерная корпускулярная инактивированная сухая представляет собой взвесь равных количеств холерных вибрионов сероваров Огава и Инаба, классических или Эль-Тор биоваров, выращенных на плотной питательной среде и инактивированных нагреванием или формалином. Препарат предназначен для активной профилактики холеры у взрослых и детей с 2-х-летнего возраста по эпидемическим показаниям.
Вакцина холерная (холероген-анатоксин в сочетании с О-антигеном) представляет собой препарат, полученный из культуры холерного вибриона 569 В серовара Инаба, инактивированный формалином. Основным действующим началом является холероген-анатоксин и соматический О-антиген. Препарат предназначен для создания активного иммунитета против холеры с 7-летнего возраста по эпидемическим показаниям.
Данные вакцины обеспечивают развитие иммунитета у 50-80% привитых продолжительностью до 6-12 мес.
С учетом недостаточной эффективности и короткого срока действия имеющихся вакцин, в настоящее время разрабатываются препараты на основе живых аттенуированных штаммов возбудителя.
Неспецифические санитарно-гигиенические мероприятия направлены на предупреждение заноса холеры из неблагополучных районов, раннее выявление больных и носителей, эпидемиологический надзор за источниками водоснабжения, контроль за соблюдением санитарно-гигиенических норм на предприятиях пищевой и молочной промышленности, торговли и т.п.
Вибрионы
Вибрионы (лат. Vibrio) — род бактерий семейства Vibrionaceae, включает более 40 видов.
Прямые или изогнутые палочки (0,4—0,7 × 1,5—2,3 мкм). Подвижны, подвижность обеспечена одним или несколькими жгутиками, расположенными полярно (моно- и лофотрихи). Спор и капсул не образуют, однако большинство видов покрыто снаружи оболочкой, образованной выростом наружного слоя клеточной стенки.
По Граму представители рода окрашиваются отрицательно, большинство видов оксидаза-положительно. Среди представителей рода наиболее распространены факультативные анаэробы. В медицинской литературе описано, что возникновению и распространению вибрионов на водных объектах способствует содержание азота более 1 мг на 1 л воды, а закисление вод обратимо ведёт к гибели микроорганизмов.
Некоторые представители рода, такие как Vibrio cholerae — галофильны, то есть могут развиваться в жидких питательных средах, содержащих до 25 % NaCl.
На данный момент фиксируют чувствительность данной группы микроорганизмов к так называемым «вибриостатикам» (англ. Vibriostatic agents). К ним относят 2,4-диамино-6,7-диизопропилптеридин и его гомологи.
Наибольший медицинский интерес представляют (помимо V. cholerae):
- Патогенные для человека: Vibrio parahaemolyticus, Vibrio vulnificus
- Патогенные для рыб: Vibrio splendidus, Vibrio ordali, Vibrio anguillarum, Vibrio tubiashi, Vibrio alginolyticus
- У ракообразных: Vibrio harveyi, Vibrio splendidus
- У головоногих моллюсков: Vibrio alginolyticus, Vibrio harveyi, Vibrio parahaemolyticus, Vibrio carchariae
V. vulnificus для человека наиболее фатальна. Зачастую развиваются такие осложнения, как септицемия и острые уретриты, острые кардиоваскулиты и целлюлиты. Наиболее часто встречается в странах Африки. Был зафиксирован случай заражения при использовании в бытовых целях воды из водоёма, который гиппопотамы предпочитали для купания.
Vibrio cincinnatiensis выделяется в клинической картине ещё и менингитами и энцефалитами, сопровождаемыми галлюцинаторной симптоматикой.
При исследовании секционного материала, поражённого некоторыми штаммами вибрионов, может наблюдаться свечение тканей в темноте.
У рыб скрытый период болезни может быть до 14 суток, его продолжительность зависит от температуры воды. Очень часто вибриоз протекает остро, бессимптомно, но может протекать и в хронической форме. Во внутренних органах нет какой-либо характерной патологии.
У креветок темнеет спина, краснеют конечности, они становятся вялыми, больные особи отказываются от корма. В сердце очаги некроза. На жабрах коричневые, красные пятна, мышцы непрозрачные, гемолимфа свёртывается. При поражении креветок некоторыми штаммами вибрионов наблюдается свечение тканей креветок в темноте. В некоторых случаях при вибриозах креветок происходит эрозия панциря. Процесс начинается с появления коричневых пятен величиной до 2 мм, потом они чернеют и сливаются, образуя очаги некроза.
У поражённых вибриозом головоногих моллюсков на теле появляются тёмные участки, развивается острый или хронический дерматит. У осьминогов наблюдается поражение глаз и внезапная гибель. У каракатиц — поражение покровов спинной части мантии, с образованием гематом.
Литература
- Воробьев «Атлас по микробиологии» ч. 1 гл. 3
- Юнчис «Некоторые малоизвестные заболевания аквариумных рыб»
- Albert, M.J., Epidemiology, genetics, and ecology of toxigenic Vibrioses . Microbiol Mol Biol Rev. (1992 March)
- Вибрион // Большая советская энциклопедия : в 66 т. (65 т. и 1 доп.) / гл. ред. О. Ю. Шмидт. — М. : Советская энциклопедия, 1926—1947.
Примечания
- Атлас по медицинской микробиологии, вирусологии и иммунологии / Под ред. А. А. Воробьева, А. С. Быкова. — М.: Медицинское информационное агентство, 2003. — С. 52. — ISBN 5-89481-136-8.
Ссылки
В Викисловаре есть статья «вибрион»
- bacterio.cict.fr
- meduniver.com
- Род Vibrio (англ.) в Мировом реестре морских видов (World Register of Marine Species).
Для улучшения этой статьи желательно:
Пожалуйста, после исправления проблемы исключите её из списка параметров. После устранения всех недостатков этот шаблон может быть удалён любым участником. |
| |
Это заготовка статьи по бактериологии. Вы можете помочь проекту, дополнив её. |
человека
специфичность
размножение
>Холерный вибрион
Факторы патогенности холерного вибриона
 , , , , , , , ,
, , , , , , , ,
Хемотаксис холерного вибриона
С помощью этих свойств вибрион вступает во взаимодействие с эпителиоцитами. У мутантов холерного вибриона (утративших способность к хемотаксису) вирулентность значительно снижается, у мутантов Mob (утративших подвижность) либо полностью исчезает, либо резко снижается.
Факторы адгезии и колонизации, с помощью которых вибрион прилипает к микроворсинкам и колонизирует слизистую оболочку тонкого кишечника. К факторам адгезии относятся муциназа, растворимая гемагглютинин/протеаза, нейраминидаза и др. Они способствуют адгезии и колонизации, так как разрушают вещества, входящие в состав слизи. Растворимая гемагглютинин/протеаза способствует отделению вибрионов от рецепторов эпителиоцитов и их выходу из кишечника во внешнюю среду, обеспечивая им эпидемическое распространение. Нейраминидаза укрепляет связь холерогена с эпителиоцитами и облегчает проникновение токсина внутрь клеток, что усиливает тяжесть диареи.
Холерный токсин — холероген.
Так называемые новые токсины, которые способны вызывать диарею, но не имеют генетического и иммунологического родства с холерогеном.
Дермонейротические и геморрагические факторы. Природа этих токсических факторов и их роль в патогенезе холеры изучены недостаточно.
 , , , , ,
, , , , ,
Эндотоксины холерного вибриона
Липополисахариды V. cholerae обладают сильным эндоток-сическим свойством и вызывают общую интоксикацию организма.
Главный из перечисленных факторов патогенности холерного вибриона — экзотоксин холероген (СТХ АВ), который и обусловливает патогенез этой болезни. Молекула холерогена состоит из двух фрагментов — А и В. Фрагмент А состоит из двух пептидов — A1 и А2, он обладает специфическим свойством холерного токсина и наделяет его качествами суперантигена. Фрагмент В состоит из 5 одинаковых субъединиц. Он выполняет две функции: 1) распознает рецептор (моносиалоганглиозид) энтероцита и связывается с ним; 2) формирует внутримембранный гидрофобный канал для прохождения субъединицы А. Пептид А2 служит для связывания фрагментов А и В. Собственно токсическую функцию выполняет пептид Aj (АДФ-рибозилтрансфераза). Он взаимодействует с НАД, вызывает его гидролиз; образующаяся при этом АДФ-рибоза связывается с регуляторной субъединицей аденилатциклазы. Это ведет к угнетению гидролиза ГТФ. Возникающий комплекс ГТФ + аденилатциклаза вызывает гидролиз АТФ с образованием цАМФ. (Другой путь накопления цАМФ — подавление холерогеном фермента, гидролизующего цАМФ до 5-АМФ). Проявление Функции гена ctxAB, кодирующего синтез экзотоксина, зависит от функции ряда Других генов патогенности, в частности генов tcp (кодирующих синтез токсин-контролируемых пилей адгезии — ТКПА), регуляторных генов toxR, toxS и toxT, генов hap (растворимой гемагглютенин/протеазы) и пей (нейраминидазы). Поэтому генетический контроль патогенности V. cholerae имеет сложный характер.
Как выяснилось, в хромосоме V. cholerae имеются два острова патогенности. Один из них представляет собой геном нитевидного умеренного конвертирующего фага СТХф, а другой — геном тоже нитевидного умеренного конвертирующего фага VPIcp. Каждый из этих островов патогенности содержит кассеты генов указанных профазе, которые и определяют патогенность возбудителя холеры. Профаг СТХф несет гены СТХ, гены новых токсинов zot и асе, ген сер (синтез адгезина), ген ortU (синтез продукта с неизвестной функцией). В эту же кассету входят ген пей и область фага RS2, которая кодирует репликацию, а также интеграцию профага в хромосомы. Гены zot, асе и ortU необходимы для формирования фаговых вирионов при исключении профага из хромосомы возбудителя.
Профаг VPIcp несет гены tcp (кодируют продукцию пилей (белок ТКПА)), гены toxT, toxR, act (дополнительный фактор колонизации, гены мобильности (интегразы и транспозазы)). Транскрипцию генов вирулентности регулируют три гена-регулятора: toxR, toxS и toxT. Эти гены координированно, на уровне транскрипции, изменяют активность более 20 генов вирулентности, включая гены ctxAB, tcp и др. Главным геном-регулятором служит ген toxR. Его повреждение или отсутствие приводят к авирулентности или к снижению продукции холерного токсина СТХ и ТКПА более чем в 100 раз. Возможно, таким образом регулируется координированное выражение генов вирулентности в островах патогенности, образуемых умеренными конвертирующими фагами и у других видов бактерий. Установлено, что в хромосоме V. cholerae eltor присутствует еще один профаг К139, но его геном мало изучен.
Ген hap локализован на хромосоме. Таким образом, вирулентность (патогенность) и эпидемическую способность V. cholerae определяют 4 гена: ctxAB, tcp, toxR и hap.
Для обнаружения способности V. cholerae продуцировать холероген можно использовать различные методы.
Биологическая проба на кроликах. При внутримышечном введении холерных вибрионов кроликам-сосункам (возраст не более 2 нед.) у них развивается типичный холерный синдром: диарея, обезвоживание и гибель кролика.
Непосредственное обнаружение холерогена с помощью ПЦР, ИФМ или реакции пассивного иммунного гемолиза (холероген связывается с Gmj эритроцитов, и они при добавлении антитоксических антител и комплемента лизируются). Однако обнаружения только способности продуцировать токсин недостаточно для определения эпидемической опасности таких штаммов. Для этого необходимо выявить наличие гена hap, поэтому лучше и надежнее всего дифференцировать токсигенные и эпидемические штаммы холерных вибрионов серогрупп 01 и 0139 с помощью ПЦР с применением специфических праймеров для обнаружения всех 4 генов патогенности: ctxAB, tcp, toxR и hap.
Способность V. cholerae, не относящихся к серогруппам 01 или 0139, вызывать спорадические или групповые диарейные заболевания у людей может быть связана либо с наличием у них энтеротоксинов типа LT или ST, стимулирующих аденилат или гуанилатциклазные системы соответственно, либо с наличием только генов ctxAB, но отсутствием гена hap.
Во время седьмой пандемии выделялись штаммы V. cholerae с различной степенью вирулентности: холерогенные (вирулентные), слабо холерогенные (маловирулентные) и нехолерогенные (невирулентные). Нехолерогенные V. cholerae, как правило, проявляют гемолитическую активность, не лизируются холерным диагностическим фагом ХДФ(5) и не вызывают заболевания человека.
Для фаготипирования V. cholerae 01 (в том числе и эльтор) С. Мукерджи были предложены наборы фагов, которые затем в России были дополнены другими фагами. Набор таких фагов (1-7) позволяет выделить среди V. cholerae 0116 фаготипов. Для идентифицирования токсигенных и нетоксигенных V. cholerae эльтор вместо ХДФ-3, ХДФ-4 и ХДФ-5 теперь в России предложены фаги СТХ* (лизируют токсигенные вибрионы эльтор) и СТХ» (лизируют нетоксигенные вибрионы эльтор).
 , , , , ,
, , , , ,
Резистентность возбудителей холеры
Холерные вибрионы хорошо выживают при низкой температуре; во льду сохраняют жизнеспособность до 1 мес; в морской воде — до 47 сут., в речной — от 3-5 дней до нескольких недель, в кипяченой минеральной воде сохраняются более 1 года, в почве — от 8 дней до 3 мес, в свежих испражнениях — до 3 сут., на вареных продуктах (рис, лапша, мясо, каши и др.) выживают 2-5 дней, на сырых овощах — 2-4 дня, на фруктах — 1-2 дня, в молоке и молочных продуктах — 5 дней; при хранении на холоде срок выживания увеличивается на 1-3 дня; на полотняном белье, загрязненном испражнениями, сохраняются до 2 сут., а на влажном материале — неделю. Холерные вибрионы при температуре 80 °С погибают через 5 мин, при 100 °С — моментально; высокочувствительны к кислотам; под влиянием хлорамина и других дезинфектантов погибают через 5-15 мин. Они чувствительны к высушиванию и действию прямых солнечных лучей, но хорошо и долго сохраняются и даже размножаются в открытых водоемах и сточных водах, богатых органическими веществами, имеющих щелочную рН и температуру выше 10- 12 °С. Высокочувствительны к хлору: доза активного хлора 0,3-0,4 мг/л воды за 30 мин вызывает надежное обеззараживание от холерного вибриона.
Патогенные для человека вибрионы, не относящиеся к виду Vibrio Cholerae
К роду Vibrio относится более 25 видов, из которых помимо V. cholerae по крайней мере следующие восемь способны вызывать заболевания у людей: V. раrаhaemolyticus, V. alginolyticus, V. vulnificus, V. fluvialis, V. fumissii, V. mimicus, V. damsela и V. hollisae. Все эти вибрионы являются обитателями морей и заливов. Заражение ими происходит либо при купании, либо при употреблении в пищу продуктов морского происхождения. Как выяснилось, холерные и не холерные вибрионы могут вызывать не только гастроэнтериты, но и раневые инфекции. Эта способность обнаружена у V. cholerae 01- и не 01-групп, у V. parahaemolyticus, V. alginolyticus, V. mimicus, V. damsela и V. vulnificus. Они вызывают воспалительные процессы в мягких тканях при повреждении их панцирем морских животных или при прямом контакте с инфицированной морской водой.
Из числа перечисленных патогенных нехолерных вибрионов наибольший практический интерес представляют V. parahaemolyticus, V. alginolyticus, V. vulnificus и V. fluvialis.
V. parahaemolyticus — парагемолитический вибрион — впервые был выделен в Японии в 1950 г. во время большой вспышки пищевой токсикоинфекции, вызванной употреблением полувысушенных сардин (летальность составила 7,5 %). Принадлежность возбудителя к роду Vibrio была установлена Р. Саказаки в 1963 г. Он разделил изученные штаммы на 2 вида: V. parahaemolyticus и V. alginolyticus. Оба вида обнаруживаются в прибрежной морской воде и у ее обитателей, они являются галофилами (греч. hals — соль); в отличие от обычных вибрионов, галофильные не растут на средах без NaCl и хорошо размножаются при высоких концентрациях ее. Видовую принадлежность галофильных вибрионов определяют по их способности ферментировать сахарозу, образовывать ацетилметилкарбинол, размножаться в ПВ с 10 % NaCl. Все эти признаки присущи виду V. alginolyticus, но отсутствуют у V. parahaemolyticus.
Парагемолитический вибрион имеет три типа антигенов: термолабильные жгутиковые Н-антигены, термостабильные, не разрушающиеся при нагревании до 120 °С в течение 2 ч О-антигены и поверхностные К-антигены, разрушающиеся при нагревании. Свежевыделенные культуры V. parahaemolyticus имеют хорошо выраженные К-антигены, которые предохраняют живые вибрионы от агглютинации гомологичными О-сыворотками. Н-антигены у всех штаммов одинаковы, но Н-антигены монотрихов отличаются от Н-антигенов перитрихов. По О-антигену V. parahaemolyticus разделяют на 14 серогрупп. Внутри серогрупп вибрионы подразделяют на серотипы по К-антигенам, общее количество которых составляет 61. Антигенная схема V. parahaemolyticus разработана применительно только к его штаммам, выделяемым от людей.
Патогенность V. parahaemolyticus связана сего способностью синтезировать гемолизин, обладающий энтеротоксическим свойством. Последнее выявляется с помощью метода Канагавы. Сущность его заключается в том, что патогенные для человека V. parahaemolyticus вызывают четкий гемолиз на кровяном агаре, содержащем 7 % NaCl. На кровяном агаре, содержащем менее 5 % NaCl, гемолиз вызывают многие штаммы V. parahaemolyticus, а на кровяном агаре с 7 % NaCl — только штаммы с энтеропатогенными свойствами. Парагемолитический вибрион обнаружен на побережьях Японского, Каспийского, Черного и других морей. Он вызывает пищевые токсикоинфекции и дизентериеподобные заболевания. Заражение происходит при употреблении в пищу сырых или полусырых морских продуктов, инфицированных V- parahaemolyticus (морская рыба, устрицы, ракообразные и т. п.).
Среди выше указанных восьми видов нехолерных вибрионов наиболее патогенным для человека является V. vulnificus, который впервые был описан в 1976 г. как Beneckea vulnificus, а затем в 1980 г. переклассифицирован в Vibrio vulnificus. Он часто обнаруживается в морской воде и ее обитателях и служит причиной различных заболеваний человека. Штаммы V. vulnificus морского и клинического происхождения не отличаются друг от друга ни фенотипически, ни генетически.
Раневые инфекции, вызываемые V. vulnificus, быстро прогрессируют и ведут к образованию опухолей с последующим некрозом ткани, сопровождаются лихорадкой, ознобом, иногда сильными болями, в некоторых случаях требуют ампутации.
V. vulnificus обнаружена способность продуцировать экзотоксин. В опытах на животных установлено, что возбудитель вызывает сильные местные повреждения с развитием отека и некроза ткани с последующим летальным исходом. Роль экзотоксина в патогенезе болезни изучается.
Помимо раневых инфекций, V. vulnificus может вызывать пневмонию у тонувших людей и эндометриты у женщин после пребывания их в морской воде. Наиболее тяжелой формой инфекции, вызываемой V. vulnificus, является первичная септицемия, связанная с употреблением в пищу сырых устриц (возможно, и других морских животных). Это заболевание развивается очень быстро: у больного появляются недомогание, лихорадка, озноб и прострация, затем сильная гипотония, являющаяся главной причиной смерти (летальность около 50 %).
V. fluvialis впервые как возбудитель гастроэнтерита был описан в 1981 г. Он относится к подгруппе нехолерных патогенных вибрионов, у которых есть аргининди-гидролаза, но неторнитин- и лизиндекарбоксилаз (V. fluvialis, V. furnissii, V. damsela, т. е. фенотипически сходных с Aeromonas). V. fluvialis — частый возбудитель гастроэнтеритов, которые сопровождаются сильной рвотой, поносом, абдоминальными болями, повышением температуры и сильной или средней тяжести дегидратацией. Главным фактором патогенности является энтеротоксин.
86) Холерный вибрион. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •Подготовка материала для окраски
- •Фиксация
- •Физический способ фиксации
- •Химический способ фиксации
- •Процесс окрашивания мазков
- •Микрокапсула
- •Функции капсулы
- •Окраска капсул
- •Окраска по методу Ожешко для выявления спор
- •11. Патогенные простейшие (возбудители амебиаза, токсоплазмоза, малярии). Морфологические особенности возбудителей и вызываемые ими заболевания.
- •12. Вирусы бактерий (бактериофаги)
- •13.Вирусы бактерий-(бактериофаги)
- •14. Морфология плесневых и дрожжеподобных грибов
- •15. Понятия об асептике и антисептике
- •16. Действие физических факторов. Физические методы стерилизации
- •17. Действие химических факторов. Дезинфекция
- •19. Химические и физико-химические методы стерилизации
- •20. Питательные среды, их классификация. Требования, предъявляемые к ним.
- •1.2. Культуры клеток в вирусологии и методы их получения
- •1.2.2. Типы клеточных культур
- •Культуры суспензированных клеток
- •1.3. Культивирование вирусов в развивающихся куриных эмбрионах
- •1.3.1. Строение куриного эмбриона
- •1.3.2. Заражение куриного эмбриона на хорионаллантоисную оболочку
- •1.4. Культивирование вирусов путём заражения лабораторных животных
- •Классификация бактерий по типам дыхания:
- •Культивирование аэробных микроорганизмов
- •Идентификация бактерий по ферментативной активности.
- •28. Понятие об инфекции, инфекционном процессе, инфекционной болезни. Условия возникновения инфекционной болезни.
- •29. Токсины бактерий, их природа и свойства.
- •Патогенность бактерий и её факторы
- •31) Характерные особенности инфекционных заболеваний.
- •32 Виды инфекций —
- •34Классификация инфекций. По происхождению. По локализации. По количеству возбудителей. По течению. Микробоносительство.
- •2)Полиинфекции — смешанные — миксты.
- •3)Реакция нейтрализации.
- •Сложные реакции(состоят из простых).
- •5)Реакции с использованием меченых антител/антигенов
- •41.Антибиотики .Их классификация по химической структуре и спектру действия.
- •42.Принципы химиотерапии инфекционных болезней.Химиотерапевтические препараты и их общая характеристика.
- •43.Понятие о химиотерапии и хтп.Хти
- •44.Антибиотики.Общая характеристика..Историяоткрытия.Классификация по механизму действия.
- •45.Классификация антибиотиков по происхождению и спектру действия.
- •46.Классификация антибиотиков по источнику получения.Способы получения.
- •47.Осложнения при антибиотикотерапии. Их предупреждение.
- •48.Методы определения чувствительности микробов к антибиотикам.
- •1)Диффузионные методы
- •2)Методы разведения
- •49.Сульфаниламиды.Разновидности.Механизм действия.
- •50.Антимикробные химиопрепараты.Нитрофураны, фторхинолоны. Механизм действия.
- •51.Микрофлора тела человека и ее значение.
- •52. Дисмикробиоценоз. Препараты применяемые для лечения.
- •53. Изменчивость бактерий. Понятие о генотипе и фенотипе бактерий.
- •54,56. Плазмиды бактерий и их значение. Использование плазмид в генной инженерии.
- •55.Виды генетических рекомбинаций у бактерий.
- •57.Использование достижений генной инженерии в получении иммунобиологических препаратов.
- •58.Понятие о биотехнологии. Использование достижений в практической микробиологии.
- •59.Вакцины. Классификация вакцин. Требования предъявляемые к вакцинным препаратам.
- •60. Анатоксины, их получение и практическое применение.
- •61. Диагностикумы (бактериальные, эритроцитарные, вирусные), получение и использование.
- •62. Диагностические сыворотки, получение и использование.
- •64.Инактивированные, корпускулярные вакцины. Приготовление и применение. Достоинства и недостатки.
- •65. Химические (субклеточные вакцины) вакцины. Получение и применение. Роль адъювантов.
- •66.Ассоциированные и комбинированные вакцины. Достоинства.
- •67. Антимикробные сыворотки. Получение и применение.
- •68.Антитоксические сыворотки. Получение, очистка, титрование и применение.
- •69.Иммуноглобулины. Получение и применение.
- •70. Методы микробиологической диагностики инфекционных заболеваний.
- •71. Основные принципы микробиологической диагностики вирусных инфекций.
- •72. Серологический метод диагностики инфекционных заболеваний.
- •73. Понятие об иммуномодуляторах. Принцип действия. Применение.
- •74. Стафилококки. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •75. Стрептококки – возбудители гнойно- воспалительных инфекций. Классификация. Свойства. Патогенез вызываемых поражений.
- •76. Стрептококки – возбудители распираторных инфекций. Классификация. Свойства. Патогенез вызываемых поражений.
- •77. Менингококки. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •78. Гонококки. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •79. Эшерихии. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •80. Возбудители брюшного тифа и паратифа. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •82)Сальмонеллы-возбудители пищевых токсикоинфекций. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •83)Лептоспиры. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •84) Возбудитель дифтерии. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •85. Возбудители туберкулеза.Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •86) Холерный вибрион. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •87) Возбудитель урогенитального хламидиоза.Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •88) Возбудитель сибирской язвы. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •89) Возбудитель столбняка. Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •90)Возбудители газовой анаэробной инфекции.Таксономия. Свойства. Патогенез вызываемых поражений. Микробиологическая диагностика. Профилактика и лечение.
- •91. Возбудитель ботулизма- тяжелая, часто фатально заканчивающаяся пищевая токсикоинфекция.
- •97. Возбудитель бруцеллеза-
- •98.Клебсиеллы-
- •99. Синегнойная палочка
- •100. Кишечныйиерсинеоз-инфекционное заболевание, сопровождающееся диареей, узловатой эритемой, артритом.
- •3.Лечение.
- •2.Лабораторная диагностика.
- •112. Аденовирусы.
- •113. Вирус эпидимического паротита.
- •114. Возбудитель ветряной оспы.
- •115. Возбудитель геморрагической лихорадки. Таксономия. Характеристика. Микробиологическая диагностика. Специфическая профилактика и лечение.
- •117.Возбудители дерматомикозов (эпидермомикозы).
- •120.Возбудитель токсоплазмоза. Таксономия. Характеристика. Микробиологическая диагностика. Лечение.
- •Вопрос 121
- •Вопрос 122
- •125. Исследование воздуха аптек
- •126. Исследование посуды, пробок, прокладок
- •127. Исследование воды для приготовления лек средств
- •128.Источники и пути загрязнения лек.Средств.
- •129. Санитарно-показательные микробы почвы и их определение
- •130. Микрофлора почвы. Санитарно-эпидемическое значение . Определение общего колличества микробов в почве.
- •131. Понятие о санитарно – показательных микроорганизмов.
- •132. Способы повышения микробной чистоты нестерильных лекарственных средств.
- •133. Бактериологическое исследование стерильных лек.Средств.
- •134. Санитарно-микробиологическое исследование инвентаря, оборудования, рук и санитарной одежды работников аптек
- •135.Методы контроля микробной загрязненности растительного лек.Сырья
- •136. Санитарно-микробиологическое исследование сухих веществ, используемых для приготовления лек.Форм.
- •138. Санитарно-микробиологическое исследование воздуха в аптеках.
- •143.При проведении исследования определяют
Возбудитель холеры
Холера – особо опасная, карантинная инфекционная болезнь, вызываемая некоторыми представителями вида Vibrio cholerae, характеризующаяся поражением тонкой кишки, нарушением водно-солевого обмена и интоксикацией. Холерный вибрион был выделен в 1883 г. Р. Кохом от больного холерой. В 1906 г. на карантинной станции Эль-Тор в Египте при обследовании паломников Ф. и У. Готшлихи выделили вибрион Эль-Тор.
Таксономия. Холерный вибрион относится к отделу Gracilicutes-, семейству Vibrionaceae, роду Vibrio. Внутри вида Vibrio cholerae различают 2 основных биовара: biovar cholerae classic (выделенный Р. Кохом) и biovar eltor (открытый Ф. и Е. Готшлихами).
Морфология и тинкториальные свойства. Холерный вибрион – небольшая грамотрицательная изогнутая палочка длиной 2-4 мкм, толщиной 0,5 мкм, не образует спор, не имеет капсулы, монотрих и чрезвычайно подвижен.
Культивирование. V. cholerae – факультативный анаэроб, но предпочитающий аэробные условия, поэтому на поверхности жидкой питательной среды образует пленку. Оптимальная температура для роста 37ºС, наиболее благоприятное значение рН среды в отличие от других микроорганизмов равно 8,5-9,0. Холерный вибрион – очень неприхотливый микроорганизм: растет на простых питательных средах, таких как 1 % щелочная лептонная вода, щелочной агар. Эти среды являются элективными для него. Характерной особенностью V. cholerae является быстрый рост – пленка на поверхности жидкой среды образуется через 6-8 ч. На плотной среде образует мелкие голубоватые колонии.
Ферментативная активность. Биохимическая активность холерного вибриона достаточно высока; он обладает большим набором ферментов. При идентификации наиболее важным является определение его отношения к маннозе, арабинозе и сахарозе. По способности ферментировать эти углеводы Хейберг все вибрионы семейства Vibrionaceae разделил на 8 групп; холерный вибрион относится к 1-й группе (манноза+, арабиноза-, сахароза+).
Антигенная структура. Холерный вибрион имеет О- и Н-анти-гены; в зависимости от строения О-антигена у него различают более 150 серогрупп. Возбудитель холеры относится к серогруппам О1 и О139 (его обозначение V. cholerae O1 и V. cholerae 0139), все другие представители вида V. cholerae не являются возбудителями холеры, но могут вызывать, например, гастроэнтериты. О-антиген состоит из 3 компонентов: А, В и С. В зависимости от их сочетания различают 3 серовара возбудителя холеры – Огава (АВ), Инаба (АС) и Гикошима (ABC). Н-анти-ген неспецифичен для V. cholerae, он является общим для всего рода Vibrio.
Факторы патогенности. Холерный вибрион образует эндотоксин. Кроме того, он выделяет экзотоксин, состоящий из нескольких фракций, наиболее важной из которых является холероген. Холероген вызывает гиперсекрецию воды и хлоридов в просвет кишечника, нарушение обратного всасывания натрия, в результате возникает диарея, приводящая к обезвоживанию организма. Экзотоксин обладает также цитотоксическим действием и вызывает гибель клеток эпителия тонкой кишки. У возбудителя холеры имеются ферменты агрессии – фибринолизин, гиалуро-нидаза, лецитиназа, нейраминидаза. Патогенность связана также с адгезивными свойствами (белки наружной мембраны), подвижностью вибриона. Дифференциация биоваров clolerae и eltor, сходных по всем перечисленным свойствам, производится с помощью ряда тестов; наиболее важные из них – чувствительность к специфическим бактериофагам, полимиксину и агглютинации куриных эритроцитов.
Резистентность. Более устойчивым к нагреванию, действию солнечных лучей, дезинфицирующим средствам является биовар eltor, хотя его резистентность сравнительно невысока. Очень чувствителен холерный вибрион к кислотам.
Восприимчивость животных. Животные к возбудителю холеры нечувствительны.
Эпидемиология. Холера – заболевание, известное с древних времен, но до начала XIX в. она встречалась только в Индии, где существовал постоянный очаг инфекции, сохраняющийся и в настоящее время. В 1817 г. очередная эпидемия холеры в Индии впервые вышла за ее пределы и охватила многие страны. В 1817-1926 гг. было 6 пандемий холеры; с 1961 г. началась седьмая пандемия, причиной которой явился биовар eltor. В настоящее время регистрируется восьмая пандемия, вызванная V. cholerae 0139 biovar eltor. Холера встречается более чем в 90 странах всех континентов, кроме Антарктиды. Это антропоноз-ная инфекция; источником инфекции являются больные люди и носители (носительство биовара eltor встречается значительно чаще, чем биовара clolerae). Механизм передачи инфекций – фекально-оральный, среди путей передачи преобладает водный, однако возможны пищевой и контактно-бытовой.
Патогенез. Вибрионы, попадающие через рот в желудок, в результате действия соляной кислоты могут погибнуть. Однако при поступлении большого количества возбудителей и снижении кислотности желудочного содержимого (разбавление его водой, пищей, гастрит со сниженной кислотностью) вибрионы попадают в тонкую кишку, размножаются, прикрепляясь к ее эпителию, и выделяют экзотоксин, который нарушает водно-солевой обмен, приводит к резкому обезвоживанию организма и ацидозу. Испражнения, состоящие из жидкости и погибших клеток слизистой оболочки, имеют вид рисового отвара. При гибели вибрионов освобождается эндотоксин, вызывающий интоксикацию.
Клиническая картина. Инкубационный период продолжается от 1 до 6 дней. Заболевание развивается остро – с повышения температуры тела, рвоты, поноса (испражнения и рвотные массы имеют вид рисового отвара). Эта стадия продолжается 1-3 дня, затем заболевание может или закончиться (при легкой форме холеры) или перейти в следующую стадию – стадию гастроэнтерита (форма средней тяжести), когда усиливаются рвота и понос, больной теряет до 30 л жидкости в сутки. Резкое обезвоживание приводит к нарушениям сердечно-сосудистой, дыхательной систем, судорогам. Затем заболевание может перейти в третью стадию (тяжелая форма холеры) – холерного алгида (от лат. algidus – холодный), характерным признаком которого является снижение температуры тела до 34ºС. Холерный алгид заканчивается смертью больного. Биовар eltor в отличие от биовара cholerae чаще вызывает заболевание, протекающее в легкой форме.
Иммунитет, вероятно, непрочный и непродолжительный.
Микробиологическая диагностика. Материалом для исследования являются рвотные массы, испражнения, пищевые продукты, вода. Как ориентировочный может быть использован бактериоскопический метод. В основном применяют бактериологический метод, позволяющий идентифицировать возбудителя (определить V. cholerae O1 или 0139), установить чувствительность к антибиотикам, провести внутривидовую идентификацию – выявление биовара и серовара. Экспресс-диагностику холеры производят с помощью РИФ.
Лечение. Назначают антибиотики широкого спектра действия и вводят плазмозамещающие жидкости.
Профилактика. Главные профилактические мероприятия – неспецифические санитарно-гигиенические и карантинные. Для специфической профилактики, имеющей вспомогательное значение, применяют холерную убитую вакцину и холерную комбинированную вакцину, состоящую из двух компонентов: холерогена-анатоксина и О-антигена холерного вибриона.